UV-VIS-Spektroskopie
Titelblatt
Felodipin
UV/VIS-Spektroskopie
WiSe 2022/2023
Abgabedatum
09.01.2023
Expertengruppe 03
Laura Schöneberg
Daniya Al Shabb
Jascha Abrahamczik
Anwendungsbeispiel der UV/VIS-Spektroskopie aus dem Europäischen Arzneibuch. Monographiebeispiel: Felodipin (Ph. Eur. 10.0/1013)
Prüfung auf Identität von Felodipin mit der UV/VIS-Spektroskopie
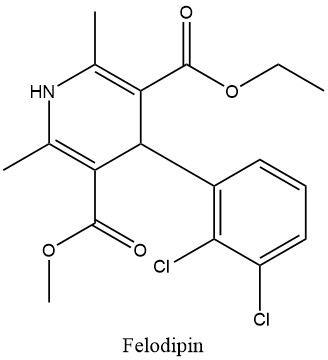
Abbildung 1: Felodipin1
Inhaltsverzeichnis
Stoffcharakterisierung
Eigenschaften
Felodipin (Summenformel: C18H19Cl2NO4), ist ein weißes bis hellgelbes kristallines Pulver, welches so gut wie unlöslich in Wasser, dafür aber löslich in organischen Lösemitteln wie Aceton oder Dichlormethan ist.2 Bei allen Synthesevorgängen entsteht das Racemat3.
Wirkungsmechanismus und Indikation
Felodipin gehört zur Gruppe der Calciumkanal–Blocker vom 1,4-Dihydropyridin-(Nifedipin-)Typ.4 Die Wirkung basiert auf allosterischer Blockade (allosterisch = es kommt zu einer Konformationsänderung des Enzyms, sodass das aktive Zentrum inaktiviert wird) des langsamen Calcium-Ioneneinstroms in die Zelle durch Calciumkanäle. Eine Depolarisation der Zytoplasmamembran erhöht die Wahrscheinlichkeit der Kanäle, geöffnet zu sein. Dies wird durch Felodipin verhindert.5
Anwendung findet Felodipin vor allem bei Hypertonie, da die Verminderung des peripheren Gefäßwiderstands zur Blutdrucksenkung führt. Des Weiteren lässt sich eine indirekte Entlastung des Herzens beobachten, da die Nachlast und im geringen Maße die Vorlast reduziert werden. Wie andere Calciumkanalblocker kann Felodipin auch bei Koronarspasmen (plötzliches Zusammenkrampfen der Koronargefäße) eingesetzt werden, da auch die größeren Koronararterien erschlaffen. Felodipin weist damit eine Gefäßselektivität auf, da eine Beeinflussung der myokardialen Kontraktilität oder der Erregungsbildung und -leitung des Herzens nicht stattfindet.6
Patienten, die von Hypertonie oder hypertropher obstruktiver Kardiomyopathie betroffen sind, erfahren durch die Einnahme von Felodipin eine arterielle Blutdrucksenkung in Ruhe und unter Belastung. Zudem nimmt auch der linksventrikuläre Füllungsdruck ab.
Durch Senkung der Nachlast des Herzens und Erhöhung der Herzfrequenz kommt es zur Steigerung des Herzzeitvolumens, welche jedoch ohne erhöhten Sauerstoffbedarf einhergeht, da die Nachlast reduziert wurde.
Des Weiteren verringert Felodipin die Natrium–Rückresorption in der Niere und übt so einen milden diuretischen Effekt aus.7
Versuchsdurchführung
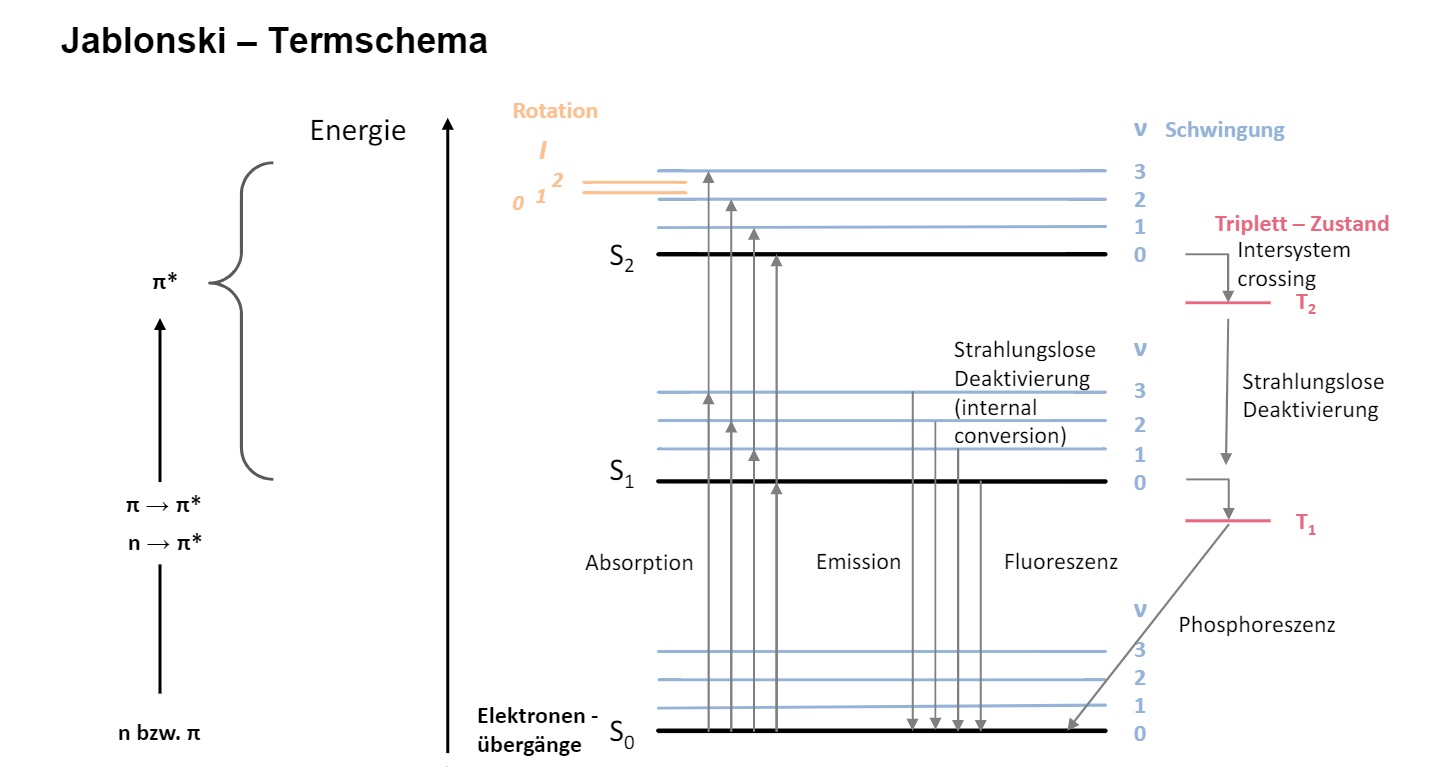
Abbildung 2: Jablonski-Termschema8
Die UV-VIS-Spektroskopie ist eine vom Arzneibuch vorgeschlagene Methode zur qualitativen sowie quantitativen Analyse und Strukturaufklärung.
Dabei bedient sich die UV-VIS-Spektroskopie der Fähigkeit von Atomen, Molekülen und Ionen, Licht in einem spezifischen Wellenlängenbereich zu absorbieren. Der nutzbare Wellenlängenbereich dieser Methode erstreckt sich über den ultravioletten (ca. 180-400 nm) und den sichtbaren (ca. 400-800 nm) Bereich.9
Die bei der Absorption aufgenommene Energie der Strahlung kann zur Anregung des Moleküls führen, welches in einen energiereicheren Zustand überführt wird. Dies ist auf Elektronenübergänge von Valenzelektronen zurückzuführen. So kann beispielsweise ein Elektron aus einem π -Orbital auf das π*-Orbital angehoben werden. Aber auch andere Übergänge sind möglich (siehe: Jablonski-Termschema)10 Genaueres zu Elektronenübergängen ist hier zu finden.
Entscheidend für die UV/VIS-Spektroskopie ist das Vorhandensein eines oder mehrerer Chromophore. Ein Chromophor ist der Teil eines Moleküls, welcher für die Absorption von UV/VIS-Licht verantwortlich ist. In organischen Molekülen sind dies die konjugierten Doppelbindungen, die das Chromophor bilden. Je länger das System aus konjugierten Doppelbindungen ist, desto weniger Energie wird für den Übergang in den angeregten Zustand benötigt.11
Der Übergang des Elektrons findet dabei von dem energetisch höchsten besetzten Molekülorbital (HOMO) zu dem energetisch niedrigsten unbesetzten Molekülorbital (LUMO) statt.12
Zudem beeinflussen auxochrome Gruppen innerhalb eines Moleküls das Chromophor. Diese funktionelle Gruppen können, wenn sie in Konjugation zu einem Chromophor stehen, das Absorptionsmaximum zum Beispiel in den langwelligeren Bereich verschieben. Dies wird dann als bathochromer Effekt bezeichnet.13
Als Messinstrument dient ein UV-Spektrometer, welches innerhalb eines resultierenden Spektrums die Absorption, bzw. die Transmission, also die Intensität der Strahlung, die nach Durchgang der Probe noch vorhanden ist, gegen die Wellenlänge aufträgt.14 Aus diesem Spektrum lassen sich die Absorptionsmaxima ablesen, die unter anderem in diesem Beispiel eine wichtige Rolle zur Identifizierung des Felodipins spielen. Für die vom Ph. Eur. vorgeschriebene UV/VIS-spektroskopische Untersuchung der Identität existieren zwei verschiedene Möglichkeiten:
- Prüfung A nach Ph. Eur.
Für die erste, schneller durchzuführende Variante werden 50 mg Substanz in Methanol R zu 100 ml gelöst. Davon werden 3 ml entnommen und mit Methanol R zu 100 ml verdünnt. Als nächstes wird ein Spektrum im Bereich von 220 bis 400 nm aufgenommen. Bei Vorhandensein von Felodipin sollten dem Spektrum zwei Absorptionsmaxima zu entnehmen sein, einmal bei 238 nm und bei 361 nm. Das Absorptionsverhältnis sollte bei 0,34 – 0,36 liegen.15 - Prüfung D nach Ph. Eur.
Für die zweite im Arzneibuch aufgeführte Möglichkeit werden 150 mg Substanz in einer Mischung von 25 ml tert-Butanol R und 25 ml Perchlorsäure-Lösung R gelöst. Nach Zugabe von 10 ml 0,1 molarer Cer(IV)–sulfat Lösung wird das Gemisch 15 min lang stehen gelassen. Anschließend wird die Lösung nach Zusatz von 3,5 ml konzentrierter Natriumhydroxid Lösung R mit verdünnter Natriumhydroxid Lösung R neutralisiert. Die erhaltene Lösung wird mit 25 ml Dichlormethan R ausgeschüttelt, und die untere Phase auf dem Wasserbad zur Trockne eingedampft. Etwa 20 mg des Rückstands werden in Methanol R zu 50 ml gelöst. 2 ml dieser Lösung werden erneut mit Methanol R zu 50 ml verdünnt. Die anschließende Messung wird bei einem Spektralbereich von 220-400 nm aufgenommen. Das entstehende Absorptionsmaximum sollte bei 273 nm liegen.17 Das für das Absorptionsmaximum verantwortliche Pyridin-Derivat (siehe Abbildung 2) geht aus der Oxidation durch Cer(IV) hervor.18
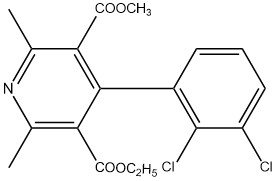
Abbildung 3: Pyridin-Derivat 16
Auswertung/ Interpretation/ Bedeutung und Eignung
Felodipin enthält konjugierte Doppelbindungen und somit ein Chromophor. Dies macht die Absorption von Licht möglich, weshalb auch die UV/VIS-spektrometrische Prüfung auf Identität geeignet ist.
Wenn die Absorptionsmaxima bei den geforderten 238 und 361 nm, bzw. den 273 nm (Prüfung D) liegen und das Absorptionsverhältnis korrekt ist, kann mit ziemlich hoher Wahrscheinlichkeit die Prüfung auf Identität als Entsprechend gekennzeichnet werden.
Gerade Prüfung A eignet sich gut zur Feststellung der Identität, da die Probenvorbereitung minimal und die Messung daher schnell und einfach durchführbar ist. Zudem ist sie deutlich weniger fehleranfällig. Vor der Messung ist zu überprüfen, ob Systemeignungsprüfungen für das Spektrometer durchgeführt worden sind, um die korrekte Funktion gewährleisten zu können. Diese Eignungsprüfungen umfassen kritische Parameter wie Wellenlängenrichtigkeit, die Absorptionsrichtigkeit, das Streulicht und die photometrische Linearität.19
Diese Überprüfungen sollten unbedingt regelmäßig durchgeführt werden, da Fehlerquellen so drastisch reduziert werden können.
Übungsaufgaben
Multiple Choice (MC) Frage: Absorption
Durch Absorption von elektromagnetischer Strahlung kann es zur Anregung von Molekülen kommen. Welche Aussagen stimmen?
- Im Grundzustand befindliche Elektronen können auf höhere Energieniveaus angehoben werden.
- Elektronen auf höheren Energieniveaus gehen durch die Anregung in den energetischen Grundzustand über.
- Es kommt zu Übergängen der Elektronen vom σ*- zum σ-Orbital
- Es kommt zu Übergängen der Elektronen vom π- zum π*-Orbital
- nur 1
- nur 2 und 3
- nur 1 und 4
- nur 1,2 und 4
- 1 bis 4 (alle)
Antwort : C
Die Absorption der elektromagnetischen Strahlung sorgt dafür, dass Moleküle angeregt werden. Diese Anregung äußert sich in einem Übergang von Valenzelektronen auf ein erhöhtes Energieniveau, welches nach sehr kurzer Verweildauer wieder, durch z.B. strahlungslose Deaktivierung, verlassen wird. Grundsätzlich können σ-Elektronen, π-Elektronen und n-Elektronen durch Anregung mit Licht auf nicht-besetzte (anti-bindende) Molekülorbitale (π*- und σ*-Orbital) angehoben werden, welche ein höheres Energieniveau aufweisen.
Multiple Choice (MC) Frage: Molarer Absorptionskoeffizient
Zur Messung wurden 9,96 mg Diisopropylketon in einem 100-ml-Messkolben eingewogen und mit Ethanol aufgefüllt. Die molare Masse der Verbindung beträgt 114 g/mol. Die Messung erfolgte mit einer Küvette mit einer Schichtdicke von einem Zentimeter. Dem Spektrum ist zu entnehmen, dass die Verbindung bei 300 nm ein Maximum mit einer Absorption von 0,3 aufweist. Berechnen Sie den molaren Absorptionskoeffizienten von Diisopropylketon.
- 340,3 l/mol⋅cm
- 0,344 l/mmol⋅cm
- 343,4 l/mol⋅cm
- 34,34 ml/mmol⋅cm
- 43,34 ml/mol⋅cm
Antwort : C
Eλ = − lg (Φ a)/(Φ e)= ελ ⋅c (X)⋅d
Durch Umformen der Gleichung nach ε erhält man mit
c (X) = 0,00996 g /114 g/mol⋅0,1 l = 0,000874 mol/l
ε λ = E λ / c (X)⋅d = 0,3 / 0,000874 mol/l ⋅ 1 cm = 343,4 l/mol⋅cm
Eλ: Absorption bei der Wellenlänge λ
Φa: austretende Strahlungsleistung in W
Φe: eingedrungene Strahlungsleistung in W
ελ: molarer Absorptionskoeffizient in l/mol·cm
c(X): Stoffmengenkonzentration in mol/l
d: Schichtdicke der Lösung in cm
Textaufgabe

Abbildung 4: Felodipin20
- Besitzt Felodipin auxochrome Gruppen? Wenn ja, welche?
Lösung: Felodipin besitzt auxochrome Gruppen: Zum einen sind es die beiden Cl-Atome. Diese verfügen über einen -I-Effekt (der den +M-Effekt überwiegt) und verringern somit das delokalisierte π-Elektronensystem. Dies führt zu einer Verschiebung des Absorptionsmaximums in den kurzwelligeren Bereich. Man spricht von einer hypsochromen Verschiebung. Zudem besitzt der Stickstoff in der Dihydropyridinstrucktur auxochrome Eigenschaften. 21
- Welchen Effekt kann man bei Molekülen mit Substituenten, die über freie Elektronenpaare verfügen, beobachten und warum?
Lösung: Auxochrome Gruppen, wie -OH, -NH2,-OR und -NR2-Gruppen verschieben das Absorptionsmaximum in den langwelligeren Bereich, auch bathochromer Effekt genannt. Grund sind die +M Effekte dieser Gruppen, da diese zu einer Vergrößerung des delokalisierten π-Elektronensystems führen, was zu einer Verringerung der benötigten Anregungsenergie führt.22
- Worin liegt der Unterschied und Vorteil eines Zweistrahlphotometers im Gegensatz zu einem Einstrahlphotometer?
Lösung: Bei einem Zweistrahlphotometer können im Gegensatz zum Einstrahlphotometer Probe und Referenz gleichzeitig vermessen werden. Dies hat zum Vorteil, dass sich die Messung schneller durchführen lässt und dass sich die Richtigkeit erhöht, da Fehler durch falsche Bedienung minimiert werden können.23
- Welchen Einfluss hat ein saurer pH–Wert auf die Absorption?
Lösung: Bei saurem pH-Wert werden basische Substanzen protoniert und liegen dadurch geladen vor. Dies führt zu einer Verringerung der Delokalisation der π–Elektronen. Das Absorptionsmaximum verschiebt sich demnach in den kürzerwelligen und damit energiereicheren Wellenlängenbereich. Dies bezeichnet man als hypsochrome Verschiebung.24
- Wie verändert sich das Auflösungsvermögen, wenn der Austrittsspalt am Monochromator verkleinert wird?
Lösung: Über den Austrittsspalt ist die spektrale Bandbreite einstellbar. Ein Kompromiss aus benötigter Lichtintensität (nicht zu schmal) und benötigter spektraler Auflösung (nicht zu breit) muss gefunden werden. Je schmaler der Austrittsspalt, desto monochromatischer wird das Licht und desto besser wird das Auflösungsvermögen.25
Einzelnachweise
Diese Quellen wurden verwendet.
1 eigene Grafik (erstellt mit Chemdraw); Urheber: J. Abrahamczik ⇑
2 Ph. Eur. 10.0/1013 Felodipin ⇑
3 Kommentar zu Ph. Eur. 4.00/1013 Felodipin ⇑
4 Kommentar zu Ph. Eur. 4.00/1013 Felodipin ⇑
5 Kommentar zu Ph. Eur. 5.0/0627 Nifedipin ⇑
6 Kommentar zu Ph. Eur. 4.00/1013 Felodipin ⇑
7 Kommentar zu Ph. Eur. 4.00/1013 Felodipin ⇑
8 Instrumentelle Analytik (Skript): Optische Methoden: UV/VIS-Spektroskopie, Kellner, T., 2022, Folie:18 ⇑
9 Ph. Eur. 10.0/2.02.25.00 UV/VIS-Spektroskopie ⇑
10 Kommentar zu Ph. Eur. 10.0/2.02.25.00 UV/VIS-Spektroskopie ⇑
11 Instrumentelle Analytik (Skript): Optische Methoden: UV/VIS-Spektroskopie, Kellner, T., 2022, Folie:25f. ⇑
12 https://www.studysmarter.de/schule/chemie/organische-chemie/chromophor/. Letzter Zugriff: 08.01.2023 ⇑
13 Instrumentelle Analytik (Skript): Optische Methoden: UV/VIS-Spektroskopie, Kellner, T., 2022, Folie:26f. ⇑
14 Ph. Eur. 10.0/2.02.25.00 UV/VIS-Spektroskopie ⇑
15 Ph. Eur. 10.0/1013 Felodipin ⇑
16 eigene Grafik (erstellt mit Chemdraw); Urheber: J. Abrahamczik ⇑
17 Ph. Eur. 10.0/1013 Felodipin ⇑
18 Kommentar zu Ph. Eur. 4.00/1013 Felodipin ⇑
19 Ph. Eur. 10.0/2.02.25.00 UV/VIS-Spektroskopie ⇑
20 eigene Grafik (erstellt mit Chemdraw); Urheber: J. Abrahamczik ⇑
21 https://www.abiweb.de/organische-chemie/farbstoffe-und-farbigkeit/farbstoffe/auxochrome.html. Letzter Zugriff: 08.01.2023 ⇑
22 https://www.chemie.de/lexikon/Auxochrom.html. Letzter Zugriff: 29.11.2022 ⇑
23 Instrumentelle Analytik (Skript): Optische Methoden: UV/VIS-Spektroskopie, Kellner, T., 2022, Folie:10 ⇑
24 Instrumentelle Analytik (Skript): Optische Methoden: UV/VIS-Spektroskopie, Kellner, T., 2022, Folie:34 ⇑
25 Instrumentelle Analytik (Skript): Optische Methoden: UV/VIS-Spektroskopie, Kellner, T., 2022, Folie:9 ⇑