Infrarot-Spektroskopie
Titelblatt
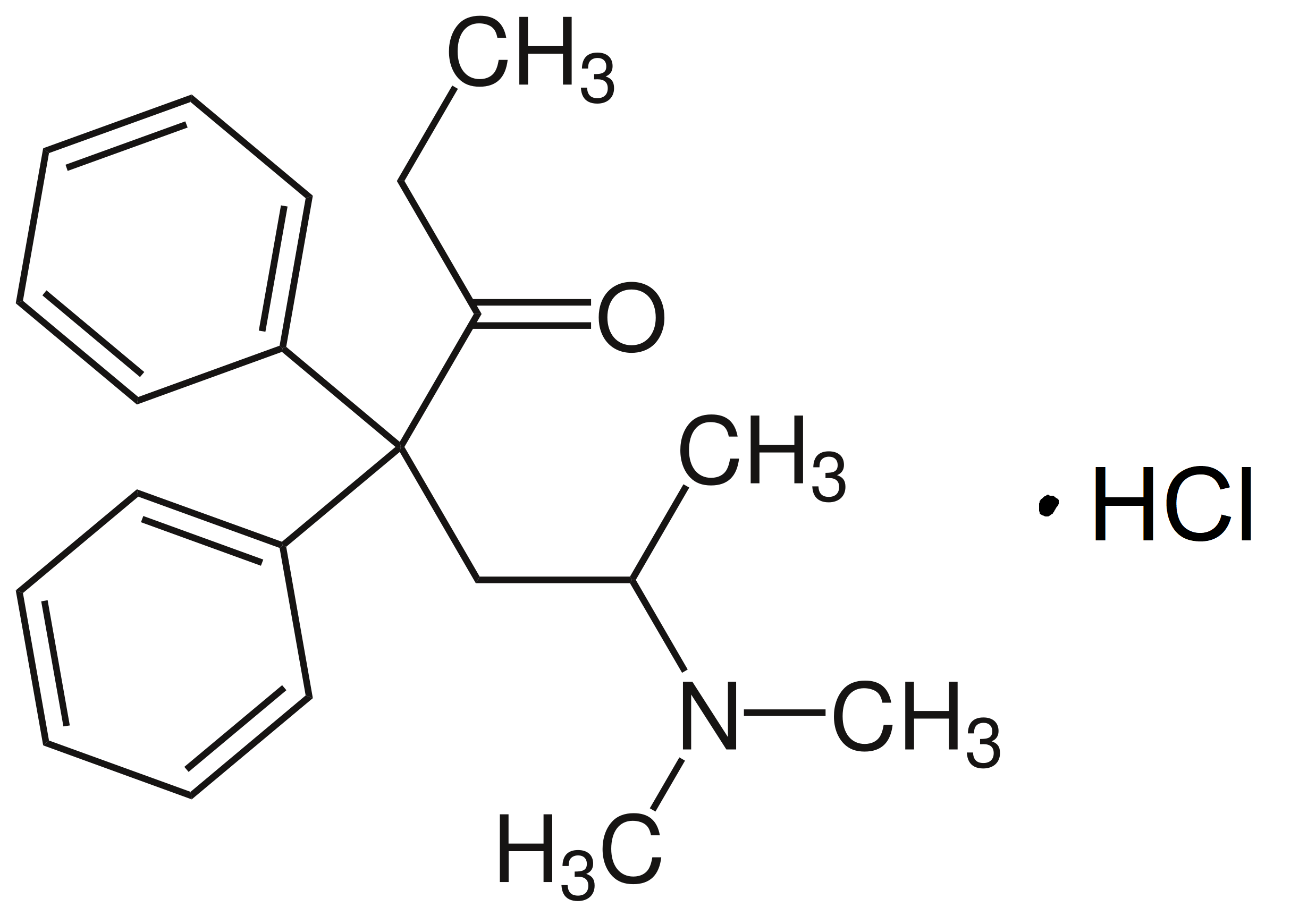
Name: Methadonhydrochlorid1
Summenformel: C21H27NO • HCl
Molare Masse: 345,9 g/mol
pKs-Wert: 8,252
Aussehen:
weißes bis fast weißes, kristallines Pulver
Schmelzpunkt:
233-236 °C
Löslichkeit:
löslich in Wasser
leicht löslich in Ethanol 96 %
Methadonhydrochlorid
IR-Spektroskopie
WiSe 2022/2023
Abgabedatum
09.01.2023
Expertengruppe 05
Mohamed Al Allam
Umut Deniz Erdogan
Taher Alassad
Lasse Harder
Anwendungsbeispiel der IR-Spektroskopie aus dem Europäischen Arzneibuch.
Prüfung auf Identität von Methadonhydrochlorid mit der IR-Spektroskopie
Inhaltsverzeichnis
Alle Lösungen sind eingeblendet. Alle Lösungen ausblenden
Stoffcharakterisierung
Methadonhydrochlorid ((6RS)-6-(Dimethylamino)-4,4-diphenylheptan-3-on-hydrochlorid) ist ein synthetisch hergestelltes Opioid, welches chiral ist und als Racemat von zwei Enantiomeren, dem Levomethadon ((R)-Methadonhydrochlorid) und dem Dextromethadon ((S)-Methadonhydrochlorid), vorkommt.3
Methadonhydrochlorid besitzt zwei Wirkmechanismen.
Es wirkt zum einen als Agonist an den µ-Opioidrezeptoren im menschlichen Gehirn und löst dabei ähnliche Wirkungen und Nebenwirkungen wie Morphin aus. Die Wirkungen nach der peroralen Einnahme als Tablette oder Sirup treten aufgrund der lipophilen Substanzeigenschaften und einer damit verbundenen längeren Plasmahalbwertszeit langsamer und langanhaltender im ZNS auf. Daher kann Methadonhydrochlorid die Entzugssymptomatik von beispielsweise intravenös appliziertem Heroin verhindern, löst jedoch keinen Rausch aus.
Methadonhydrochlorid wird daher in der Substitutionstherapie bei Heroinabhängigen eingesetzt.4
Des Weiteren hemmt Methadonhydrochlorid als Antagonist die Reizweiterleitung an den NMDA-Rezeptoren und kann daher auch als Analgetikum bei chronischen Schmerzen eingesetzt werden. Das linksdrehende (R)-Methadon weist dabei eine deutlich höhere analgetische Wirkung auf.5
Versuchsdurchführung
Die Identität des Wirkstoffs Methadonhydrochlorid wird durch die IR-Spektroskopie untersucht. Diese unterteilt sich in 3 Teilbereiche (NIR, MIR und FIR). Genutzt wird IR-Strahlung im mittleren Bereich der Wellenzahlen von 4000 cm-1 bis 200 cm-1 (das entspricht Wellenlängen von 2,5 µm bis 50 µm). Die mittlere IR-Strahlung ist langwellig und reicht nicht mehr aus, um ein Elektron auf ein höheres Molekülorbital anzuheben, ist aber energiereich genug, um die Moleküle in Schwingung zu versetzen. Es gibt 3 Arten von Schwingungen (Valenz-, Deformations- und Gerüstschwingungen). Bei der Valenzschwingung kommt es zur Dehnung und Stauchung einer Bindung und bei der Deformationsschwingung kommt es zur Deformation eines Bindungswinkels. Die sogenannten Gerüstschwingungen kommen durch Schwingungen des gesamten Molekülgerüstes zustande. Dadurch bekommt man für jedes organische Molekül ein einzigartiges IR-Spektrum.6
In der Durchführung dieser instrumentellen Methode verwenden wir ein Fourier-Transform-Gerät, welches ein Einstrahlgerät ist. Anstelle eines Gittermonochromators bzw. eines Prismen-Monochromators besitzt dieses Gerät ein Interferometer, welches sich zwischen Lichtquelle und Probe befindet.7
Methadonhydrochlorid kann in einer Lösung und in fester Form untersucht werden. Im Nachfolgenden beschäftigen wir uns mit der festen Substanz als Probe mit Kaliumbromid als Trägermaterial. Kaliumbromid ist im Vergleich zu Glas oder Quarzglas IR-durchlässig und nicht IR-aktiv.8
Die Voraussetzung für die Absorption der IR-Strahlung (IR-Aktivität) ist, dass das Molekül entweder ein veränderbares oder ein induzierbares Dipolmoment aufweist.9
Die Probe wurde wie folgt untersucht:

KBr-Pressling10
Die Probe muss trocken sein, da durch Wasser die Messergebnisse verfälscht werden können.
2,0 mg der Probe und 998,0 mg von Kaliumbromid werden mit einem Mörser und einem Pistill gründlich verrieben und pulverisiert. Anschließend werden 600 mg der erhaltenen Mischung zu einer 13 mm dünnen Scheibe bei einem Druck von 1300 bar in einem Presswerkzeug zu einem Pressling verarbeitet. Das Presswerkzeug übt etwa 5-10 Minuten Druck auf das Pulver aus, wodurch die KBr-Körner zu einer plastischen Scheibe werden.11
Der fertige Pressling wird mit einer Pinzette entnommen und sollte nicht mit den Händen angefasst werden, da der Pressling durch das Hautfett verunreinigt werden kann, was sich auf das Spektrum auswirken könnte. Um die Durchlässigkeit unseres Presslings zu prüfen, wird die Scheibe gegen eine Lichtquelle gehalten und durchgeschaut. Es dürfen sich am Rand leichte Trübungen befinden.
Zu Beginn wird der Untergrund bei freiem Strahlengang aufgenommen. Danach wird der Pressling in die Pressling-Halterung gelegt und in das Spektrometer eingesetzt. Die verschiedenen Schwingungsvarianten der Moleküle werden durch Messung der Transmission ermittelt und man erhält am Ende einen Ausdruck (Bandenspektrum).12
Bei Entsorgung des Presslings nach der Messung ist zu beachten, dass es sich hier um ein Betäubungsmittel handelt und die missbräuchliche Verwendung ausgeschlossen werden muss. Daher wird die Probe unter Aufsicht zerkleinert, in heißem Wasser gelöst oder aufgeschwemmt und dann mit Hilfe von Zellstoff aufgenommen. Die Entsorgung erfolgt dann über den Feststoffabfall.13
Auswertung/ Interpretation/ Bedeutung und Eignung
Zur Identifizierung von Methadonhydrochlorid mittels IR-Spektroskopie fordert das Europäische Arzneibuch einen Vergleich des Spektrums der Probe mit dem Referenzspektrum.14 Da es sich bei Methadonhydrochlorid um ein Betäubungsmittel handelt und CRS-Proben von Betäubungsmitteln Beschränkungen unterliegen, wird nur das CRS-Referenzspektrum des kristallinen Feststoffs Methadonhydrochlorid als Racemat zum Vergleich herangezogen. Dies führt jedoch zu Abweichungen, wenn man das in Deutschland handelsübliche Methadon, das (R)-Methadonhydrochlorid, bestimmen möchte.15
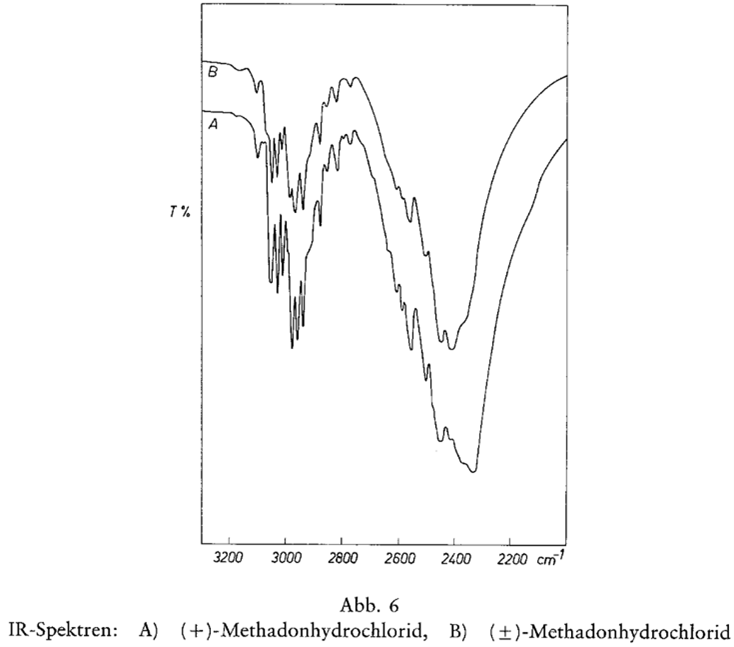
IR-Spektren zum Vergleich zwischen Racemat und Enantiomer 16
Der Unterschied macht sich bemerkbar im Bereich der Wellenzahlen von 2300-2400 cm-1 und geringfügig im Wellenzahlenbereich von 2900-3100 cm-1.17 Es werden die Bandenpositionen, die Anzahl der Maxima und Minima sowie die relativen Größen der Banden von Probe und Referenzspektrum miteinander verglichen.18
Dabei eignet sich der Fingerprintbereich, der im Wellenzahlenbereich von 1500-500 cm-1 liegt, besonders gut, weil jedes Molekül hier ein einzigartiges Bandenspektrum aufweist. Jedoch kann man im Fingerprintbereich, im Gegensatz zum Funktionsbereich 4000-1500 cm-1, den Banden keine bestimmten funktionellen Gruppen zuordnen.
Bei der Messung kann es zu verschiedenen Messstörungen kommen. Beispielsweise können Streuverluste der Probe zu einer schiefen Basislinie führen, welche sich leicht ausgleichen lässt. Ebenfalls kann das hygroskopische Kaliumbromid, wenn es Wasser aus der Umgebungsluft gezogen hat, Wasserbanden bei einer Wellenzahl von 3400-3200 cm-1 auslösen. Wenn ein zu hoher Druck ausgeübt wird, kann es zu einer Kristallumwandlung (Polymorphie) kommen. Dies würde sich im Fingerprintbereich bemerkbar machen.19
Außerdem schreibt das Arzneibuch neben der IR-spektroskopischen Prüfung von Methadonhydrochlorid eine nasschemische Prüfung auf die Identität von Chlorid-Ionen mittels Fällung mit Silbernitrat vor, weil Chlorid-Ionen nicht IR-aktiv sind. Somit kann nicht ausgeschlossen werden, ob es sich nicht um ein anderes Salz desselben Wirkstoffmoleküls handelt.20
Übungsaufgaben (MC-Frage und Textaufgaben)
Multiple Choice Frage: IR-Spektrum von Methadonhydrochlorid
Welche der folgenden Aussagen zum Bandenspektrum treffen zu?
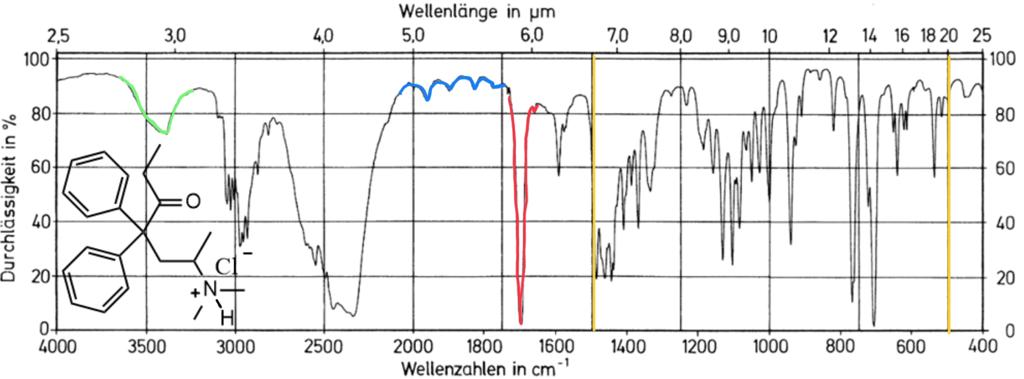
IR-Bandenspektrum zu (R)-Methadonhydrochlorid21
1) Zwischen den Wellenzahlen von 1500cm-1 und 500cm-1 liegt der Funktionsbereich.
2) Bei der Wellenzahl 1700cm-1 liegt der Bereich der Carbonylgruppe.
3) Die Wellenzahlen von 2000cm-1 bis 1800cm-1 können den Aromaten zugeordnet werden.
4) Die Bande bei einer Wellenzahl von 3400cm-1 ist einer Amino-Gruppe zuzuordnen.
5) Die Bande bei einer Wellenzahl von 3400cm-1 ist einer Wasserbande zuzuordnen.
- Nur 1.
- Nur 2 und 4.
- Nur 2, 3 und 4.
- Nur 3, 4 und 5.
- Alle (1-5) sind richtig.
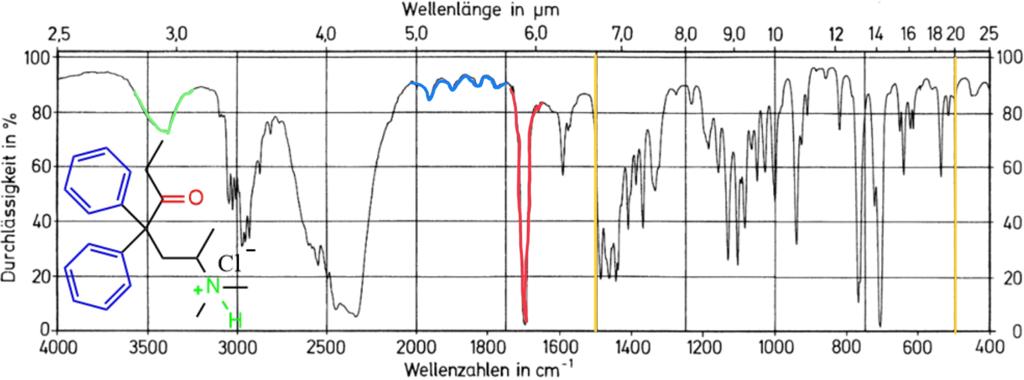
Antwort C ist korrekt.
- Zwischen den Wellenzahl von 1500 cm-1 bis 500cm-1 liegt der Fingerprintbereich.
- Die Carbonylgruppe ist bei einer Wellenzahl von 1700 cm-1 zu finden.
- Die Aromaten sind bei Wellenzahlen zwischen 2000 cm-1 und 1800 cm-1 abgebildet.
- Die Bande bei einer Wellenzahl von 3400 cm-1 ist eine Amino-Gruppe.
- Eine Wasserbande sieht wie folgt aus:
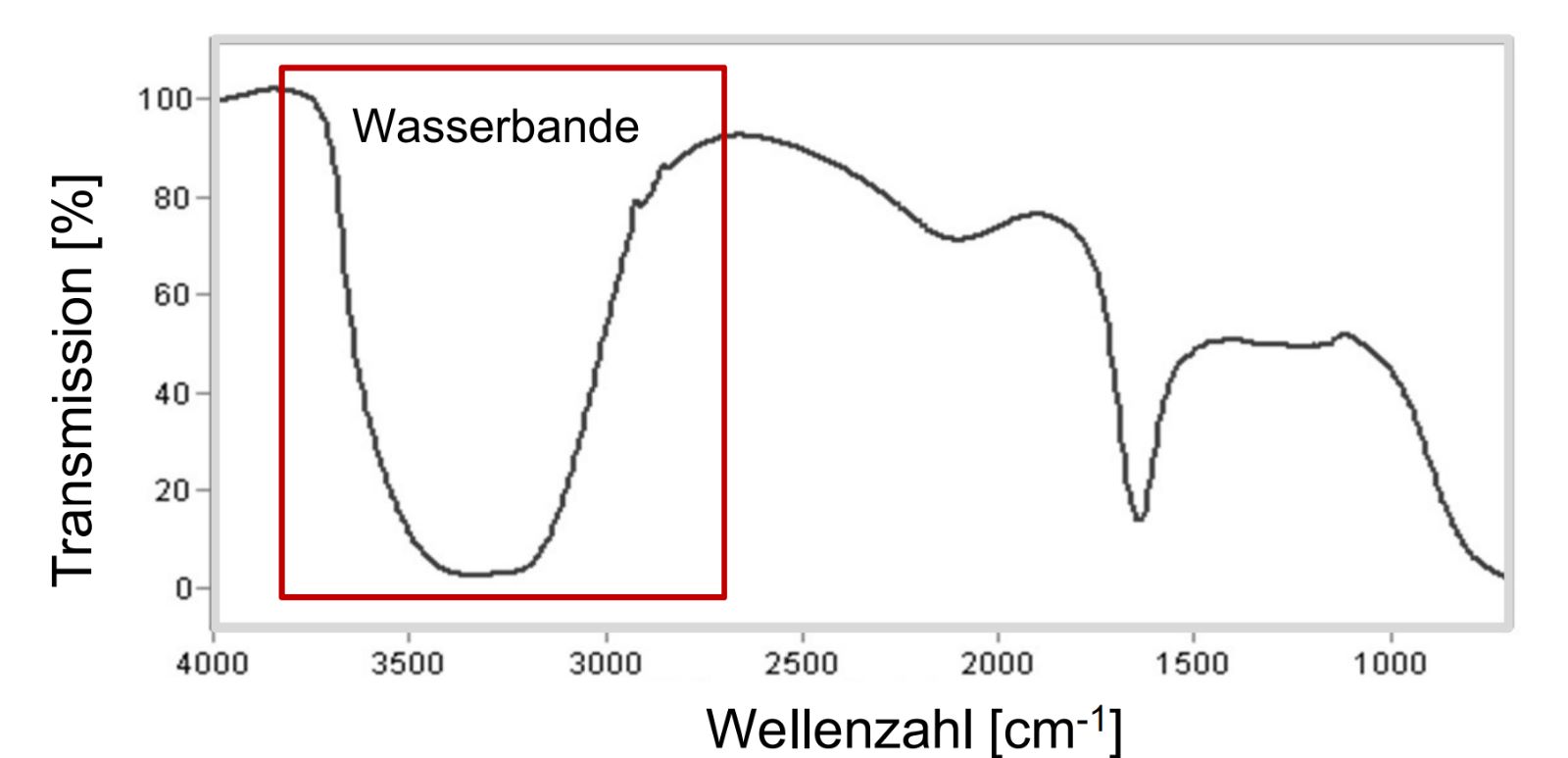
IR-Spektrum mit einer Wasserbande22
Textaufgaben: Fragen zur IR-Spektroskopie und zu unserem Anwendungsbeispiel
- Welche Schwingungsarten weisen die folgenden funktionellen Gruppen auf?
- Carbonylgruppen
- Aromaten
- Amino-Gruppen
- Carbonylgruppen: Valenzschwingung (C=O) (1700 cm-1)
- Aromaten: Gerüstschwingungen (1700-2500 cm-1)
- Amino-Gruppen: Valenzschwingungen (N-H) (3400 cm-1)
- Welche Trägermaterialien sind für die IR-Spektroskopie geeignet und warum sind diese geeignet?
Hauptsächlich werden anorganische Salze wie Halogenide der Alkalimetalle verwendet. Die gängigsten Trägermaterialien sind Kaliumbromid, Natriumchlorid und Lithiumfluorid, da sie IR-durchlässig und nicht IR-aktiv sind.
- Berechnen Sie die Anzahl der Schwingungsmöglichkeiten, die Methadonhydrochlorid besitzt und erklären Sie wovon diese abhängig sind (C21H27NO • HCl).
Z = 3 * N – 6
Z = Anzahl der Schwingungsmöglichkeiten, N = Anzahl der Atome
Z = 3 * 51 – 6 = 147 Schwingungsmöglichkeiten.
Je größer ein Molekül ist, desto mehr Schwingungsmöglichkeiten besitzt es. Diese Möglichkeiten hängen von der Anzahl der Atome im Molekül ab. Jedes Atom kann sich in 3 Raumrichtungen bewegen, d.h. die Bewegungsfreiheiten sind die Anzahl der Atome mal 3. Es gibt 2 weitere Bewegungsmöglichkeiten, die keine Schwingung in sich darstellen, jedoch die maximal möglichen Schwingungen beeinflussen. Dies sind die Translation (3 Fälle) und die Rotation (3 Fälle).23
- Warum kann der Gehalt von Methadonhydrochlorid in fester Form mit der IR-Spektroskopie nicht bestimmt werden?
Da bei den Presslingen keine fest definierte Schichtdicke vorliegt und daher keine Konzentration bestimmt werden kann.24
Einzelnachweise
1 Eigenschaften und Grafik siehe Ph. Eur. 10. Ausgabe, Grundwerk 2020, Methadonhydrochlorid ⇑
2 vgl. https://primamedchem.com/de/product/kaufen-forschungschemikalien/methadon-hcl-pulver-online-kaufen/#:~:text=235%20%C2%B0C%2C%20einen-,pKa%2DWert,-von%208%2C25%20in, Abruf: 05.01.2023 ⇑
3 vgl. Kommentar zum Ph. Eur. 5.5, 26. Lfg 2007, Methadonhydrochlorid ⇑
4 vgl. Aktories, K, Flockerzi, V, Förstermann, U, & Hofmann, FB (eds) 2022, Allgemeine und Spezielle Pharmakologie und Toxikologie, Urban & Fischer Verlag GmbH & Co. KG, Philadelphia. Available from: ProQuest Ebook Central. Abruf: 24.11.2022 ⇑
5 vgl. https://flexikon.doccheck.com/de/Methadon, Abruf: 25.11.2022 ⇑
6 vgl. Kellner, Dr. Thomas, Folien Optische Methoden: Infrarot-Spektroskopie, WiSe 22/23, S.5-7 ⇑
7 vgl. Kellner, Dr. Thomas, Folien Optische Methoden: Infrarot-Spektroskopie, WiSe 22/23, S.18 ⇑
8 vgl. Kellner, Dr. Thomas, Folien Optische Methoden: Infrarot-Spektroskopie, WiSe 22/23, S.21 ⇑
9 vgl. https://www.chemie.de/lexikon/IR-Spektroskopie.html#:~:text=in%20irgendeinem%20anderen.-,Absorption%20von%20IR%2DStrahlung,aufweist%20, Abruf: 19.12.2022 ⇑
10 Eigenaufnahme im Labor der Instrumentellen Analytik von Lasse Harder, erstellt am 29.11.2022 ⇑
11 „Infrared Spectra of Some Important Narcotics“, in: Internetseite journals.sagepub, URL: https://journals.sagepub.com/doi/abs/10.1366/000370256774633845?journalCode=aspc, Abruf am 22.11.2022 ⇑
12 vgl. Kellner, Dr. Thomas, Folien Optische Methoden: Infrarot-Spektroskopie, WiSe 22/23, S.24 ⇑
13 vgl. https://www.pharmazeutische-zeitung.de/regeln-fuer-die-apotheken-116790/seite/3/#:~:text=BTM%20k%C3%B6nnen%20%C3%BCber, Abruf: 27.12.2022 ⇑
14 vgl. Ph. Eur. 10.0/0408 Methadonhydrochlorid ⇑
15 vgl. Kommentar zum Ph. Eur. 10.3/2.02.24.00 IR-Spektroskopie ⇑
16 vgl, Mikrochimica Acta, Beitrag zur thermischen Analyse und zur Polymorphie optischer Antipoden: Pantolacton, Methadon und Usninsäure, Abbildung 6 ⇑
17 vgl. Mikrochimica Acta, Beitrag zur thermischen Analyse und zur Polymorphie optischer Antipoden: Pantolacton, Methadon und Usninsäure ⇑
18 vgl. Kellner, Dr. Thomas, Folien Optische Methoden: Infrarot-Spektroskopie, WiSe 22/23, S.48 ⇑
19 vgl. Kellner, Dr. Thomas, Folien Optische Methoden: Infrarot-Spektroskopie, WiSe 22/23, S.54 ⇑
20 vgl. Kommentar zum Ph. Eur. 10.3/2.02.24.00 IR-Spektroskopie ⇑
21 vgl. Kommentar zum Ph. Eur. 5.5, 26. Lfg 2007, Methadonhydrochlorid, inklusive mit ChemDraw erstellter Grafik zu Methadonhydrochlorid von Umut Deniz Erdogan ⇑
22 vgl. Kellner, Dr. Thomas, Folien Optische Methoden: Infrarot-Spektroskopie, WiSe 22/23, S.54 ⇑
23 vgl. Kellner, Dr. Thomas, Folien Optische Methoden: Infrarot-Spektroskopie, WiSe 22/23, S.15-16 ⇑
24 vgl. Kellner, Dr. Thomas, Folien Optische Methoden: Infrarot-Spektroskopie, WiSe 22/23, S.26 ⇑