Gaschromatographie
Titelblatt
Anwendungsbeispiel
Gaschromatographie
WiSe 2022/2023
Abgabedatum
06.01.2023
Expertengruppe 10
Johanna Dirksen
Lara Katharina Johnsen
Tamara Zastrow
Lilli Brandt
Anwendungsbeispiel der Gaschromatographie aus dem Europäischen Arzneibuch. Monographiebeispiel: Natriumvalproat (10.0/0678)
Prüfung auf Reinheit von Natriumvalproat mittels Gaschromatographie
Inhaltsverzeichnis
Alle Lösungen sind eingeblendet. Alle Lösungen ausblenden
Stoffcharakterisierung
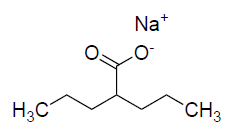
Abbildung 1: Strukturformel von Natriumvalproat 1
Natriumvalproat, auch Natrium(2-propylpentanoat) genannt, ist ein weißes bis fast weißes, polymorphes, kristallines und hygroskopisches Pulver, welches sehr leicht in Wasser und leicht in Ethanol 96% löslich ist.2 Natriumvalproat ist das Natriumsalz der kurzkettigen Fettsäure Valproinsäure (IUPAC-Name: 2-Propylpentansäure). Der Siedepunkt liegt bei 222°C.3 Der Gehalt soll laut dem Europäischen Arzneibuch zwischen 98,5% bis 101,0% liegen. Natriumvalproat gehört zu der Arzneimittelgruppe der Antikonvulsiva und wird parenteral oder peroral bei Epilepsie und Krampfanfällen angewendet, sowie in Ausnahmefällen bei der Behandlung von bipolaren Störungen zur Stimmungsstabilisierung, wenn andere Wirkstoffe kontraindiziert sind.4 5 Durch die Valproinsäure werden im Nervensystem die spannungsabhängigen Natrium- sowie Calciumkanäle blockiert, wodurch die Synthese der Gamma-Aminobuttersäure (GABA) angeregt wird. Die Valproinsäure hemmt ebenfalls die Enzyme, die für den Abbau von GABA zuständig sind. Diese Effekte führen zu einem Anstieg an GABA im Nervensystem. Bei Menschen mit Epilepsie werden die Nervenzellen im Gehirn zu stark erregt, was zu Krampfanfällen führt. 6 GABA hat eine hemmende Wirkung auf das überreizte Nervensystem.7
Versuchsdurchführung
Allgemeines zur Gaschromatographie
Die Gaschromatographie (GC) ist ein Trennverfahren, bei dem Substanzen in gas- oder dampfförmigen Zustand mit Hilfe einer gasförmigen mobilen Phase (Trägergas) und einer flüssigen oder festen stationären Phase aufgetrennt werden. Bei dieser Methode unterscheidet man zwischen einer Verteilungschromatographie (GLC- gas-liquid-chromatography) mit einer flüssigen stationären Phase und einer Absorptionschromatographie (GSC- gas-solid-chromatography) mit einer festen stationären Phase. In der pharmazeutischen Analytik überwiegt die Anwendung der Verteilungschromatographie.8
Voraussetzung für die GC ist, dass die Substanzen in den gasförmigen Zustand überführbar sind, d.h. dass die Substanzen, falls sie nicht bereits im gasförmigen Zustand vorliegen, unzersetzt verdampfbar sind. Ist diese Bedingung nicht gegeben, so muss eine Derivatisierungsreaktion durchgeführt werden um eine flüchtige Substanz zu erhalten. Ein weiteres Erfordernis ist, dass das Lösungsmittel inert ist.9 Zusätzliche Vorraussetzungen ergeben sich aus dem spezifischen Aufbau des eingesetzten Gaschromatographen. Falls z.B. als Detektor ein FID (Flammenionisationsdetektor) verwendet wird, darf das Lösungsmittel keine Verbrennungsprodukte erzeugen. Flammenionisationsdetektoren werden vor allem für die quantitative Bestimmung eingesetzt.10
Die Durchführung einer GC findet im allgemeinen wie folgt statt: Die zu analysierenden Substanzen werden im Injektor zunächst verdampft (falls notwendig) und daraufhin in den Trägergasstrom eingeführt, mit welchem sie durch eine beheizbare Trennsäule transportiert werden. In dieser findet die Substanztrennung durch Verteilung zwischen der mobilen- und der stationären Phase statt. Die schließlich eluierenden Substanzen werden durch einen Detektor angezeigt, dessen Signal durch einen Schreiber, Integrator oder PC-Auswertungssystem aufgezeichnet wird.11
Durchführung der Prüfung auf Reinheit von Natriumvalproat
Zur Herstellung der Untersuchungslösung werden zunächst 0,500 g der aus dem Natriumsalz isolierten Valproinsäure auf der Analysenwaage eingewogen.13 Daraufhin wird die Substanz in 10 ml demineralisiertem Wasser gelöst. Es werden 5 ml verdünnte Schwefelsäure hinzugegeben. Die Lösung wird mit 20 ml Heptan 3-mal im Scheidetrichter ausgeschüttelt. Nachdem die oberen Phasen vereinigt wurden, werden diese in einem Messkolben auf 100,0 ml mit Heptan aufgefüllt. Es werden zwei Referenzlösungen hergestellt: Für die Referenzlösung a werden 5 mg Valproinsäure mit der Verunreinigung K ((2RS)-2-Ethyl-2-methylpentansäure) auf einer Analysenwaage abgewogen. Die Substanz wird mit Hilfe einer Vollpipette mit 1,0 ml Heptan versetzt. Zur Herstellung der Referenzlösung b werden 1,0 ml der Untersuchungslösung mithilfe einer Vollpipette abgemessen und in einem 100,0 ml Messkolben mit Heptan aufgefüllt.
Das Europäische Arzneibuch schlägt für diese Prüfung die folgenden Komponenten für die Durchführung der Gaschromatographie vor: Es wird eine Widebore-Kapillare aus Quarzglas mit einer Länge von 30 m und einem Durchmesser von 0,53 mm verwendet. Als stationäre feste Phase dient Macrogol-20000-nitroterephthalat R mit einer Filmdicke von 0,5 µm. Als Trägergas wird Helium benötigt, dessen Durchflussrate auf 8 ml pro Minute eingestellt wird. Es werden 1 µl der zu analysierenden Lösungen auf die Säule eingespritzt. Das anzuwendende Temperaturprogramm ist in Tabelle 1 dargestellt. Außerdem wird ein Flammenionisationsdetektor verwendet. Die relative Retention der Verunreinigung K liegt bezogen auf Valproinsäure (tR etwa 17 Minuten) bei etwa 0,97.14
Auswertung/ Interpretation/ Bedeutung und Eignung
Eignung und Interpretation
Zur quantitativen Bestimmung des Arzneistoffs Natriumvalproat gibt das Arzneibuch eine GC vor.15 Bei genauerer Betrachtung des Wirkstoffs zeigen sich viele Punkte, die für eine Analyse mit Hilfe dieser Methode sprechen und diese Entscheidung des Arzneibuchs somit stützen. Natriumvalproat weist eine hohe molekulare Hitzebeständigkeit auf, welche auch für die Nutzung des FID notwendig ist. Des Weiteren ist eine Derivatisierung nicht notwendig, da die vorbereitete Analysenlösung flüchtig ist. Ebenfalls von Vorteil ist, dass mit Hilfe der Methode auch sehr ähnliche Stoffe zuverlässig aufgetrennt werden können, sodass man Valproinsäure beispielsweise von der ihr sehr ähnlichen Verunreinigung K ((2RS)-2-Ethyl-2-methylpentansäure) trennen kann. In diesem Zusammenhang ist auch die hohe Empfindlichkeit der Methode zu erwähnen, da auch kleinste Mengen von Verunreinigung so quantifiziert werden können.16 17 Ein Nachteil der Bestimmung mit Hilfe der Gaschromatographie ist die Notwendigkeit einer Kalibrierung, da die vom Projektor angezeigten Flächenprozente nicht immer mit den Gewichtsprozenten der detektierten Stoffe übereinstimmen. Dadurch wird die Anwendung der Gaschromatographie erschwert. Auch die Ermittlung eines internen Standards ist notwendig um zufällige Fehler, vor allem des Injektionssystems, auszuschließen.18
Auswertung
Das Chromatogramm wird anhand der relativen Retention von Valproat ( tR = etwa 17 Minuten) und der Verunreinigungen ausgewertet. Hierbei gibt das Arzneibuch vor, dass die Verunreinigung K im Vergleich zum Hauptpeak nicht mehr als das 0,15-fache der Fläche betragen darf. Bei unbekannten Verunreinigungen liegt der Grenzwert beim 0,05-fachen der Fläche. Die Auflösung zwischen dem Peak der Valproinsäure und der Verunreinigung K muss mindestens 2 betragen.19 20
Übungsaufgaben
Multiple Choice (MC) Frage: Lösemittel der GC
Wieso wird hier bei der Gaschromatographie als Lösungsmittel Heptan angewendet? Welche Aussage trifft nicht zu?
- Heptan ist ein inertes Lösungsmittel.
- Heptan und Valproinsäure haben unterschiedliche Siedepunkte.
- Heptan ist ein unpolares Lösungsmittel.
- Heptan ist leicht flüchtig und unzersetzt verdampfbar.
- Heptan und Valproinsäure haben denselben Siedepunkt.
Antwort 5 ist falsch. Heptan und Valproinsäure haben verschiedene Siedepunkte. Der Siedepunkt von Heptan ist deutlich niedriger. Man bevorzugt Lösungsmittel mit geringen Siedepunkten, da sie einen Lösungsmittelpeak (mit geringer Retentionszeit) bewirken, der sich dann nicht auf die Messwerte auswirken kann. 21
Textaufgabe: Allgemeines zur Gaschromatographie
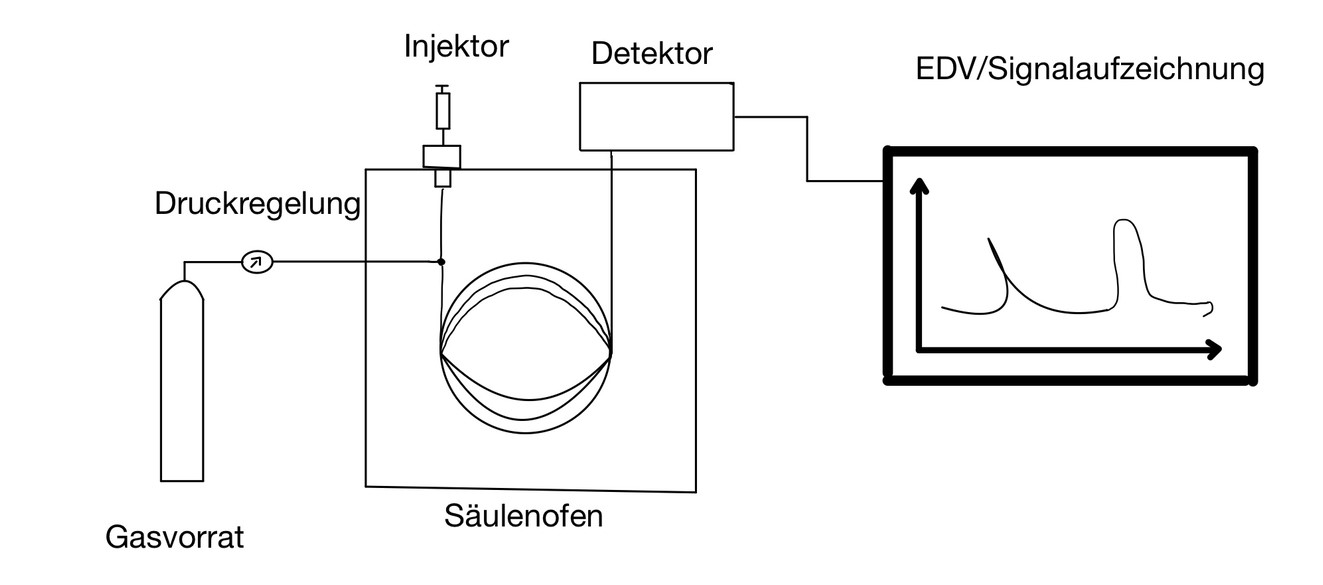
- Wie ist ein Gaschromatograph aufgebaut?
- Wo werden die Stoffe bei der Durchführung der Gaschromatographie aufgetrennt?
Die Stoffe werden in der vom Säulenofen erhitzten Säule aufgetrennt.24
- Welche Eigenschaften muss der Stoff besitzen, um optimal bei einer Gaschromatographie analysiert zu werden?
Der Stoff muss gasförmig vorliegen oder unzersetzt verdampfbar sein. Er muss zudem thermostabil und flüchtig sein. 25
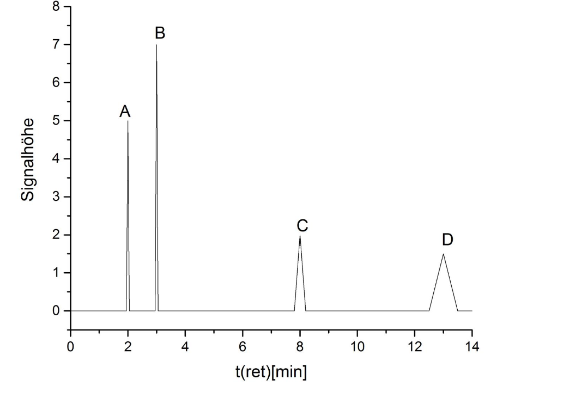
- Sie haben eine Gaschromatographie durchgeführt und das oben dargestellte Diagramm erhalten. Die Peaks C und D sind nicht optimal. Was kann angepasst werden, um die Darstellung zu optimieren?
Um die Retentionszeit zu verkürzen und die Peakform zu verbessern, wird die Temperatur erhöht(Isotherm). Falls es nun zu einer Peaküberlagerung von A und B kommt, ist ein Temperaturgradient notwendig, sodass nach der Auftrennung von A und B die Temperatur erhöht wird. 26
Einzelnachweise
verwendete Quellen:
1 eigene Grafik; Urheber: J. Dirksen ⇑
2 Europäisches Arzneibuch 10. Ausgabe, Grundwerk 2020 (Monographie: 10.0/0678) ⇑
3 https://www.chemie-schule.de/KnowHow/Valproins%C3%A4ure als letztes abgerufen am 05.01.2023, 17:07 ⇑
4 https://www.gelbe-liste.de/wirkstoffe/Natrium-valproat_26190 als letztes abgerufen am 26.11.2022, 16:50 ⇑
5 https://www.pharmawiki.ch/wiki/index.php?wiki=Valproins%C3%A4ure als letztes abgerufen am 06.01.2023, 11:27 Uhr ⇑
6 https://idw-online.de/de/news170919 als letztes abgerufen am 05.01.2023, 17:18 Uhr ⇑
7 https://www.netdoktor.de/medikamente/valproinsaeure/ als letztes abgerufen am 26.11.2022, 16:50 Uhr ⇑
8 Rücker, Neugebauer, Willems: Instrumentelle pharmazeutische Analytik, 5. Auflage. Stuttgart: Wissenschaftliche Verlagsgesellschaft mbH, 2013 S. 441 ⇑
9 Rücker, Neugebauer, Willems: Instrumentelle pharmazeutische Analytik, 5. Auflage. Stuttgart: Wissenschaftliche Verlagsgesellschaft mbH, 2013 S. 441 ⇑
10 Rücker, Neugebauer, Willems: Instrumentelle pharmazeutische Analytik, 5. Auflage. Stuttgart: Wissenschaftliche Verlagsgesellschaft mbH, 2013, S. 455-456 ⇑
11 Rücker, Neugebauer, Willems: Instrumentelle pharmazeutische Analytik, 5. Auflage. Stuttgart: Wissenschaftliche Verlagsgesellschaft mbH, 2013 S. 441-442 ⇑
12 eigene Grafik; Urheber: J. Dirksen ⇑
13 Europäisches Arzneibuch Kommentar 10. Ausgabe, Grundwerk 2020 (Monographie: 7.4/0678) ⇑
14 Europäisches Arzneibuch 10. Ausgabe, Grundwerk 2020 (Monographie: 10.0/0678) ⇑
15 Europäisches Arzneibuch 10. Ausgabe, Grundwerk 2020 (Monographie: 10.0/0678) ⇑
16 https://www.chemie.de/lexikon/Gaschromatographie.html#:~:text=Die%20Gas%2DFl%C3%BCssigkeits%2DChromatographie%20, als letztes abgerufen am 26.11.2022, 16:57 Uhr ⇑
17 Rücker, Neugebauer, Willems: Instrumentelle pharmazeutische Analytik, 5. Auflage. Stuttgart: Wissenschaftliche Verlagsgesellschaft mbH, 2013 S. 459 ⇑
18 https://www.chemie.de/lexikon/Gaschromatographie.html#:~:text=Die%20Gas%2DFl%C3%BCssigkeits%2DChromatographie%20, als letztes abgerufen am 26.11.2022, 16:57 Uhr ⇑
19 Europäisches Arzneibuch 10. Ausgabe, Grundwerk 2020 (Monographie: 10.0/0678) ⇑
20 Europäisches Arzneibuch Kommentar 10. Ausgabe, Grundwerk 2020 (Monographie: 7.4/0678) ⇑
21 https://www.analytik.ethz.ch/vorlesungen/biopharm/Trennmethoden/AnalytischeChemie_Skript_4_GC.pdf, als letztes abgerufen am 28.11.2022, 16:45 Uhr ⇑
22 Kellner, Instrumentelle Analytik, GC Skript S.18, WiSe 22/23 ⇑
23 eigene Grafik; Urheber: L. Johnsen ⇑
24 Rücker, Neugebauer, Willems: Instrumentelle pharmazeutische Analytik, 5. Auflage. Stuttgart: Wissenschaftliche Verlagsgesellschaft mbH, 2013 S. 442 ⇑
25 Rücker, Neugebauer, Willems: Instrumentelle pharmazeutische Analytik, 5. Auflage. Stuttgart: Wissenschaftliche Verlagsgesellschaft mbH, 2013 S. 441 ⇑
26 Kellner, Instrumentelle Analytik, GC Skript S.18-20, WiSe 22/23 ⇑